Контакт:Ерол Джоу (г-н)
Тел: плюс 86-551-65523315
Мобилно/WhatsApp: плюс 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Електронна поща:sales@homesunshinepharma.com
добавете:1002, Хуанмао Сграда, №105, Мънчън Път, Хефей Град, 230061, Китай
Concert Pharma е биофармацевтична компания от клиничен етап, която разработва основно лекарства с малка молекула за лечение на заболявания на централната нервна система, генетични заболявания, бъбречни заболявания, възпалителни заболявания и рак. Наскоро компанията обяви старта на първото си клинично изпитване фаза 3, THRIVE-AA1, за да оцени ефикасността и безопасността на пероралния инхибитор на JAK CTP-543 при лечението на възрастни с умерена до тежка алопеция ареата. Компанията очаква да докладва резултатите от изпитанието THRIVE-AA1 през 2022 г. Очаква се второто изпитание THRIVE-AA2 от фаза 3 да започне през първата половина на 2021 г.
През юли тази година FDA на САЩ е предоставил CTP-543 пробивно лекарство (BTD) за лечение на умерена до тежка алопеция ареата при възрастни. Алопеция ареата е автоимунно заболяване, при което имунната система атакува космените фоликули, причинявайки частична или пълна загуба на коса. Понастоящем няма лекарство, одобрено от FDA за лечение на алопеция ареата.
Д-р Джеймс В. Касела, главен директор по развитие на концерта, заяви: „Въз основа на резултатите от нашия фаза 2 проект, ние вярваме, че CTP-543 има потенциала да осигури най-добрата в класа терапия за пациенти с умерена до тежка алопеция areata. Работим усилено. Насърчавайте развитието на CTP-543, за да направите значими промени в живота на пациенти с алопеция ареата."
След края на изпитанието Фаза 2, Concert и американската FDA обсъдиха ключовата информация за проекта Фаза 3 и стратегията за регистрация и стартираха изпитанието Phase 3 THRIVE-AA1. След оценка на дозовия диапазон на CTP-543 за лечение на пациенти с умерена до тежка алопеция ареата, изпитването във фаза 2 даде положителни резултати, компанията проведе среща с FDA. Според настоящия график, компанията вярва, че положителните резултати от двете проучвания фаза 3 могат да бъдат използвани като основа за подаване на нова заявка за наркотици (NDA) за CTP-543 за лечение на умерена до тежка алопеция ареата в възрастни в началото на 2023г.
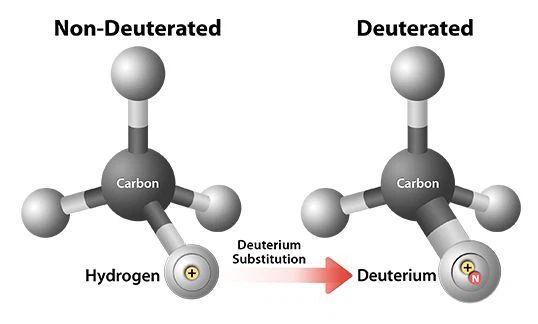
Технология за деутерация
Анди Брайънт, изпълняващ длъжността главен изпълнителен директор на Фондация за алопеция ареата, каза:" Милиони хора са засегнати от алопеция ареата. CTP-543 има потенциал да се превърне в едно от първите одобрени от FDA лекарства за лечение на алопеция ареата. Ние сме много насърчени от това."
Алопеция ареата може да доведе до отпадане на част или цялата коса по скалпа или тялото и болестта засяга до 650 000 души в САЩ. Скалпът е най-често засегнатата област, но всяка област, където расте косата, може да бъде засегната самостоятелно или с скалпа. Алопеция ареата може да се появи на всяка възраст. Повечето пациенти започват да развиват симптоми на 40-годишна възраст. Болестта засяга както жените, така и мъжете. Алопеция ареата може да има сериозни психологически последици, включително тревожност и депресия.
CTP-543 е открит чрез прилагането на деутериевата химическа технология Concert' за модифициране на руксолитиниб. Руксолитиниб е селективен инхибитор на Janus киназа 1 и Janus киназа 2 (JAK1 / JAK2). За лечение на някои кръвни заболявания. Химическата модификация на деутерия на руксолитиниб може да промени неговата човешка фармакокинетика, като по този начин засили използването му като лечение на алопеция ареата.

FDA предостави на CTP-543 пробивно лекарствено обозначение (BTD) за лечение на умерена до тежка алопеция ареата въз основа на положителните резултати от клинично проучване във фаза 2. Данните показват, че двете групи с високи дози CTP-543 (12 mg и 8 mg) са достигнали първичната крайна точка за ефикасност в сравнение с групата на плацебо: на 24-та седмица от лечението има значително по-висок дял на пациентите с инструмент за тежест на алопеция Резултат (SALT) Относителното намаляване на изходното ниво е ≥50% (съответно 58%, 47%, 9%; всички p-стойности са< 0,001).="" в="" допълнение,="" през="" 24-та="" седмица="" от="" лечението,="" значително="" по-висок="" дял="" от="" пациентите="" в="" групата="" с="" 12="" mg="" и="" 8="" mg="" в="" сравнение="" с="" групата="" на="" плацебо="" (съответно="" 42%,="" 26%,="" 7%)="" постигна="" общ="" резултат="" на="" salt="" ≤20="" (в="" сравнение="" до="" плацебо):="" съответно="">< 0,001,="">< 0,05),="" това="" е="" основната="" крайна="" точка="" за="" ефикасност,="" която="" concert="" възнамерява="" да="" използва="" в="" своето="" проучване="" за="" ключова="">
В допълнение, през 24-та седмица, в сравнение с групата на плацебо, групите за лечение с 12 mg и 8 mg CTP-543 също са постигнали значително по-големи подобрения в алопеция areata, оценени от скалата за глобално впечатление за подобрение на пациента. Конкретните данни са: 78% и 58% от пациентите в кохортата с 12 mg и 8 mg група са оценени като GG; много подобрена" или" много подобрен" съответно, което е значително в сравнение с разликата в плацебо групата. В това проучване лечението с CTP-543 обикновено се понася добре.